సూది రహిత పరికరం ఇన్సులిన్, ప్రతిరోధకాలు, RNA లేదా ఇతర పెద్ద అణువులను పంపిణీ చేయడానికి ఉపయోగించవచ్చు.
స్క్విడ్లు తమను తాము సముద్రం గుండా ముందుకు నడిపించడానికి మరియు సిరా మేఘాలను కాల్చడానికి జెట్లను ఉపయోగించే విధానం ద్వారా ప్రేరణ పొందిన MIT మరియు నోవో నార్డిస్క్ పరిశోధకులు కడుపు లేదా జీర్ణాశయంలోని ఇతర అవయవాలకు నేరుగా మందులను విడుదల చేసే ఒక జీర్ణమయ్యే క్యాప్సూల్ను అభివృద్ధి చేశారు. .
ఈ క్యాప్సూల్ ఇన్సులిన్ మరియు యాంటీబాడీస్తో సహా ఇతర పెద్ద ప్రొటీన్ల వంటి సాధారణంగా ఇంజెక్ట్ చేయాల్సిన మందులను బట్వాడా చేయడానికి ప్రత్యామ్నాయ మార్గాన్ని అందిస్తుంది. ఈ సూది-రహిత వ్యూహం మధుమేహం, ఊబకాయం మరియు ఇతర జీవక్రియ రుగ్మతలకు చికిత్స చేయడానికి వ్యాక్సిన్గా లేదా చికిత్సా అణువుగా RNAను అందించడానికి కూడా ఉపయోగించవచ్చు.
“మేము అన్వేషిస్తున్న దీర్ఘకాల సవాళ్లలో ఒకటి, సాధారణంగా ఒక ఇంజెక్షన్ ఇవ్వాల్సిన స్థూల కణాల నోటి ద్వారా పంపిణీ చేయడాన్ని ప్రారంభించే వ్యవస్థల అభివృద్ధి. ఈ పని ఆ పురోగతిలో తదుపరి ప్రధాన పురోగతిలో ఒకటి,” అని జియోవన్నీ ట్రావెర్సో చెప్పారు. , లాబొరేటరీ ఫర్ ట్రాన్స్లేషనల్ ఇంజనీరింగ్ డైరెక్టర్ మరియు MITలో మెకానికల్ ఇంజనీరింగ్ అసోసియేట్ ప్రొఫెసర్, గ్యాస్ట్రోఎంటరాలజిస్ట్ బ్రిఘం మరియు ఉమెన్స్ హాస్పిటల్లో, బ్రాడ్ ఇన్స్టిట్యూట్ యొక్క అసోసియేట్ సభ్యుడు మరియు అధ్యయనం యొక్క సీనియర్ రచయిత.
MITలోని ట్రావెర్సో మరియు అతని విద్యార్థులు బ్రిఘం మరియు ఉమెన్స్ హాస్పిటల్ మరియు నోవో నార్డిస్క్లోని పరిశోధకులతో కలిసి కొత్త క్యాప్సూల్ను అభివృద్ధి చేశారు. గ్రాహం అరిక్ SM ’20 మరియు నోవో నార్డిస్క్ శాస్త్రవేత్తలు డ్రాగో స్టిక్కర్ మరియు అగియాద్ గజల్ పేపర్కు ప్రధాన రచయితలు, ఇది ఈ రోజు కనిపిస్తుంది. ప్రకృతి .
సెఫలోపాడ్స్ ద్వారా ప్రేరణ పొందింది
పెద్ద ప్రొటీన్లు లేదా ఆర్ఎన్ఏతో కూడిన మందులు సాధారణంగా నోటి ద్వారా తీసుకోబడవు ఎందుకంటే అవి జీర్ణవ్యవస్థలో సులభంగా విరిగిపోతాయి. చాలా సంవత్సరాలుగా, ట్రావెర్సో యొక్క ల్యాబ్ అటువంటి మందులను మౌఖికంగా పంపిణీ చేసే మార్గాలపై పనిచేస్తోంది, వాటిని చిన్న పరికరాలలో నిక్షిప్తం చేయడం ద్వారా వాటిని క్షీణత నుండి కాపాడుతుంది మరియు వాటిని నేరుగా జీర్ణవ్యవస్థలోని లైనింగ్లోకి ఇంజెక్ట్ చేస్తుంది.
ఈ క్యాప్సూల్స్లో చాలా వరకు పరికరం జీర్ణాశయంలోకి వచ్చిన తర్వాత మందులను అందించడానికి చిన్న సూది లేదా మైక్రోనెడిల్స్ సెట్ను ఉపయోగిస్తాయి. కొత్త అధ్యయనంలో, ట్రావెర్సో మరియు అతని సహచరులు ఈ అణువులను ఎలాంటి సూది లేకుండా పంపిణీ చేసే మార్గాలను అన్వేషించాలని కోరుకున్నారు, ఇది కణజాలానికి ఏదైనా నష్టం కలిగించే అవకాశాన్ని తగ్గిస్తుంది.
దానిని సాధించడానికి, వారు సెఫలోపాడ్స్ నుండి ప్రేరణ పొందారు. స్క్విడ్లు మరియు ఆక్టోపస్లు తమ మాంటిల్ కేవిటీని నీటితో నింపడం ద్వారా తమను తాము ముందుకు నడిపించగలవు, తర్వాత వాటిని తమ సైఫాన్ ద్వారా వేగంగా బయటకు పంపుతాయి. నీటి బహిష్కరణ శక్తిని మార్చడం ద్వారా మరియు సైఫాన్ను వేర్వేరు దిశల్లో చూపడం ద్వారా, జంతువులు వాటి వేగం మరియు ప్రయాణ దిశను నియంత్రించగలవు. సిఫాన్ అవయవం సెఫలోపాడ్లను సిరా యొక్క జెట్లను కాల్చడానికి అనుమతిస్తుంది, మాంసాహారుల దృష్టిని మరల్చడానికి డికోయ్ మేఘాలను ఏర్పరుస్తుంది.
గుళిక నుండి ద్రవ ఔషధాలను బయటకు నెట్టడానికి అవసరమైన శక్తిని ఉత్పత్తి చేయడానికి కంప్రెస్డ్ కార్బన్ డయాక్సైడ్ లేదా గట్టిగా చుట్టబడిన స్ప్రింగ్లను ఉపయోగించి ఈ జెట్టింగ్ చర్యను అనుకరించడానికి పరిశోధకులు రెండు మార్గాలతో ముందుకు వచ్చారు. గ్యాస్ లేదా స్ప్రింగ్ కార్బోహైడ్రేట్ ట్రిగ్గర్ ద్వారా సంపీడన స్థితిలో ఉంచబడుతుంది, ఇది తేమ లేదా కడుపు వంటి ఆమ్ల వాతావరణానికి గురైనప్పుడు కరిగిపోయేలా రూపొందించబడింది. ట్రిగ్గర్ కరిగిపోయినప్పుడు, గ్యాస్ లేదా స్ప్రింగ్ విస్తరించడానికి అనుమతించబడుతుంది, క్యాప్సూల్ నుండి ఔషధాల జెట్ను బయటకు పంపుతుంది.
జీర్ణవ్యవస్థ నుండి కణజాలాన్ని ఉపయోగించి చేసిన ప్రయోగాల శ్రేణిలో, పరిశోధకులు ఔషధాలను తగినంత శక్తితో బహిష్కరించడానికి అవసరమైన ఒత్తిడిని లెక్కించారు, అవి సబ్ముకోసల్ కణజాలంలోకి చొచ్చుకుపోయి అక్కడ పేరుకుపోతాయి, ఆపై కణజాలంలోకి మందులను విడుదల చేసే డిపోను సృష్టించారు.

“షార్ప్ల తొలగింపు పక్కన పెడితే, అధిక-వేగం గల కాలమ్ జెట్ల యొక్క మరొక సంభావ్య ప్రయోజనం స్థానికీకరణ సమస్యలకు వాటి దృఢత్వం. కణజాలంతో సన్నిహిత సంబంధాన్ని కలిగి ఉండాల్సిన చిన్న సూదికి భిన్నంగా, మా ప్రయోగాలు జెట్ చేయగలదని సూచించాయి. దూరం నుండి లేదా కొంచెం కోణంలో ఎక్కువ మోతాదును అందించడానికి, “అరిక్ చెప్పారు.
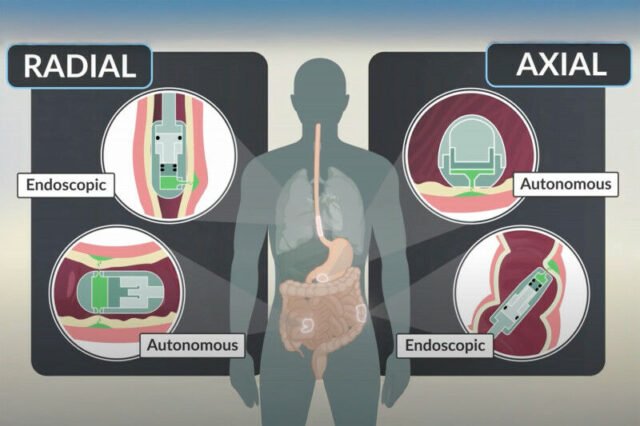
పరిశోధకులు క్యాప్సూల్స్ను కూడా రూపొందించారు, తద్వారా అవి జీర్ణవ్యవస్థలోని వివిధ భాగాలను లక్ష్యంగా చేసుకోవచ్చు. క్యాప్సూల్ యొక్క ఒక వెర్షన్, ఫ్లాట్ బాటమ్ మరియు ఎత్తైన గోపురం కలిగి ఉంటుంది, ఇది కడుపు యొక్క లైనింగ్ వంటి ఉపరితలంపై కూర్చుని, కణజాలంలోకి ఔషధాన్ని క్రిందికి విసర్జించగలదు. సెల్ఫ్-ఓరియెంటింగ్ క్యాప్సూల్స్పై ట్రావెర్సో యొక్క ల్యాబ్ నుండి మునుపటి పరిశోధనల నుండి ప్రేరణ పొందిన ఈ క్యాప్సూల్ బ్లూబెర్రీ పరిమాణంలో ఉంటుంది మరియు 80 మైక్రోలీటర్ల ఔషధాన్ని తీసుకువెళ్లగలదు.
రెండవ సంస్కరణ ట్యూబ్-వంటి ఆకారాన్ని కలిగి ఉంది, ఇది అన్నవాహిక లేదా చిన్న ప్రేగు వంటి పొడవైన గొట్టపు అవయవంలో తనను తాను సమలేఖనం చేయడానికి అనుమతిస్తుంది. అలాంటప్పుడు, ఔషధం క్రిందికి కాకుండా పక్క గోడ వైపు బయటకు పంపబడుతుంది. ఈ వెర్షన్ 200 మైక్రోలీటర్ల ఔషధాన్ని అందించగలదు.
మెటల్ మరియు ప్లాస్టిక్తో తయారు చేయబడిన, క్యాప్సూల్స్ జీర్ణవ్యవస్థ గుండా వెళతాయి మరియు వాటి డ్రగ్ పేలోడ్ను విడుదల చేసిన తర్వాత విసర్జించబడతాయి.
సూదులు లేని మందు డెలివరీ
జంతువులలో చేసిన పరీక్షలలో, పరిశోధకులు ఈ క్యాప్సూల్స్ను ఇన్సులిన్ను అందించడానికి ఉపయోగించవచ్చని చూపించారు, ఇది మధుమేహం ఔషధం Ozempic మాదిరిగానే GLP-1 రిసెప్టర్ అగోనిస్ట్ మరియు షార్ట్ ఇంటర్ఫెరింగ్ RNA (siRNA) అని పిలువబడే ఒక రకమైన RNA. ఈ రకమైన RNA జన్యువులను నిశ్శబ్దం చేయడానికి ఉపయోగించబడుతుంది, ఇది అనేక జన్యుపరమైన రుగ్మతల చికిత్సలో సమర్థవంతంగా ఉపయోగపడుతుంది.
జంతువుల రక్తప్రవాహంలో ఔషధాల సాంద్రత, సిరంజితో మందులను ఇంజెక్ట్ చేసినప్పుడు కనిపించిన అదే పరిమాణంలో స్థాయికి చేరుకుందని మరియు కణజాల నష్టాన్ని వారు గుర్తించలేదని కూడా వారు చూపించారు.
ఇన్సులిన్ లేదా ఇతర ఇంజెక్ట్ చేసిన మందులను తరచుగా తీసుకోవాల్సిన రోగులు ఇంట్లోనే జీర్ణమయ్యే క్యాప్సూల్ను ఉపయోగించవచ్చని పరిశోధకులు భావిస్తున్నారు. ముఖ్యంగా సూదులు ఇష్టపడని రోగులకు మందులు ఇవ్వడం సులభతరం చేయడంతో పాటు, ఈ విధానం పదునైన సూదులను పారవేయాల్సిన అవసరాన్ని కూడా తొలగిస్తుంది. పరిశోధకులు ఎండోస్కోప్కు జోడించగల పరికరం యొక్క సంస్కరణను కూడా సృష్టించారు మరియు పరీక్షించారు, రోగికి మందులు పంపిణీ చేయడానికి వైద్యులు దానిని ఎండోస్కోపీ సూట్ లేదా ఆపరేటింగ్ గదిలో ఉపయోగించేందుకు అనుమతించారు.
“ఈ సాంకేతికత ఇన్సులిన్ మరియు GLP-1 అగోనిస్ట్ల వంటి స్థూల కణ ఔషధాల యొక్క నోటి ద్వారా ఔషధ డెలివరీలో ఒక ముఖ్యమైన పురోగతి. గతంలో ఓరల్ డ్రగ్ డెలివరీ కోసం అనేక విధానాలు ప్రయత్నించినప్పటికీ, అవి అధిక జీవ లభ్యతను సాధించడంలో పేలవమైన సామర్థ్యాన్ని కలిగి ఉన్నాయి. ఇక్కడ, అధిక సామర్థ్యంతో జంతు నమూనాలలో జీవ లభ్యతను అందించగల సామర్థ్యాన్ని పరిశోధకులు ప్రదర్శిస్తారు, ఇది చాలా మందికి ప్రభావవంతంగా ఉంటుంది బయోలాజిక్స్ ప్రస్తుతం ఇంజెక్షన్లు లేదా ఇంట్రావాస్కులర్ ఇన్ఫ్యూషన్ల ద్వారా నిర్వహించబడుతున్నాయి” అని పరిశోధనలో పాల్గొనని రైస్ విశ్వవిద్యాలయంలో బయో ఇంజనీరింగ్ ప్రొఫెసర్ ఒమిద్ వీసే చెప్పారు.
మానవులలో వాటిని పరీక్షించాలనే ఆశతో పరిశోధకులు ఇప్పుడు క్యాప్సూల్స్ను మరింత అభివృద్ధి చేయాలని ప్లాన్ చేస్తున్నారు.