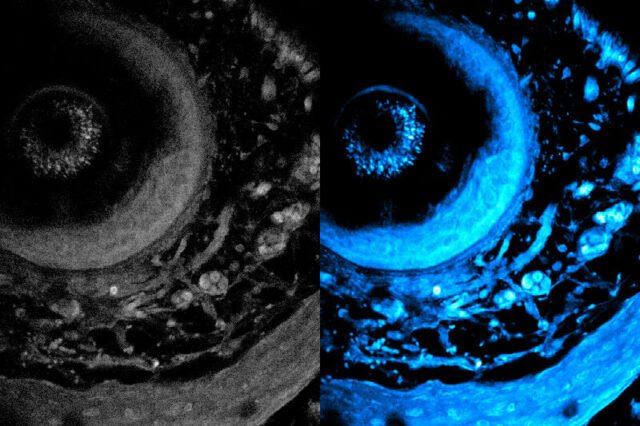
అధిక శక్తితో పనిచేసే లేజర్లను ఉపయోగించి, ఈ కొత్త పద్ధతి జీవశాస్త్రజ్ఞులు శరీరం యొక్క రోగనిరోధక ప్రతిస్పందనలను అధ్యయనం చేయడంలో మరియు కొత్త ఔషధాలను అభివృద్ధి చేయడంలో సహాయపడుతుంది.
మెటబాలిక్ ఇమేజింగ్ అనేది నాన్వాసివ్ పద్ధతి, ఇది లేజర్ లైట్ని ఉపయోగించి సజీవ కణాలను అధ్యయనం చేయడానికి వైద్యులు మరియు శాస్త్రవేత్తలను అనుమతిస్తుంది, ఇది వ్యాధి పురోగతి మరియు చికిత్స ప్రతిస్పందనలను అంచనా వేయడంలో వారికి సహాయపడుతుంది.
కానీ కాంతి జీవ కణజాలంలోకి ప్రకాశించినప్పుడు వెదజల్లుతుంది, అది ఎంత లోతుగా చొచ్చుకుపోగలదో పరిమితం చేస్తుంది మరియు సంగ్రహించిన చిత్రాల రిజల్యూషన్కు ఆటంకం కలిగిస్తుంది.
ఇప్పుడు, MIT పరిశోధకులు మెటబాలిక్ ఇమేజింగ్ యొక్క సాధారణ లోతు పరిమితిని రెట్టింపు చేసే కొత్త సాంకేతికతను అభివృద్ధి చేశారు. వారి పద్ధతి ఇమేజింగ్ వేగాన్ని కూడా పెంచుతుంది, గొప్ప మరియు మరింత వివరణాత్మక చిత్రాలను అందిస్తుంది.
ఈ కొత్త సాంకేతికతకు కణజాలాన్ని కత్తిరించడం లేదా రంగులతో మరక చేయడం వంటి వాటిని ముందుగా ప్రాసెస్ చేయాల్సిన అవసరం లేదు. బదులుగా, ప్రత్యేకమైన లేజర్ కణజాలంలోకి లోతుగా ప్రకాశిస్తుంది, దీని వలన కణాలు మరియు కణజాలాలలోని కొన్ని అంతర్గత అణువులు కాంతిని విడుదల చేస్తాయి. ఇది కణజాలాన్ని మార్చవలసిన అవసరాన్ని తొలగిస్తుంది, దాని నిర్మాణం మరియు పనితీరు యొక్క మరింత సహజమైన మరియు ఖచ్చితమైన ప్రాతినిధ్యాన్ని అందిస్తుంది.
లోతైన కణజాలాల కోసం లేజర్ కాంతిని అనుకూలీకరించడం ద్వారా పరిశోధకులు దీనిని సాధించారు. ఇటీవల అభివృద్ధి చేసిన ఫైబర్ షేపర్ని ఉపయోగించి – దానిని వంగడం ద్వారా వారు నియంత్రించే పరికరం – వారు కాంతి యొక్క రంగు మరియు పప్పులను ట్యూన్ చేయగలరు మరియు కాంతి కణజాలంలోకి లోతుగా ప్రయాణిస్తున్నప్పుడు వికీర్ణాన్ని తగ్గించడానికి మరియు సిగ్నల్ను పెంచడానికి. ఇది సజీవ కణజాలంలోకి మరింత ఎక్కువగా చూడడానికి మరియు స్పష్టమైన చిత్రాలను సంగ్రహించడానికి వారిని అనుమతిస్తుంది.
ఎక్కువ చొచ్చుకుపోయే లోతు, వేగవంతమైన వేగం మరియు అధిక రిజల్యూషన్ ఈ పద్ధతిని ప్రత్యేకంగా క్యాన్సర్ పరిశోధన, కణజాల ఇంజనీరింగ్, డ్రగ్ డిస్కవరీ మరియు రోగనిరోధక ప్రతిస్పందనల అధ్యయనం వంటి డిమాండ్ ఇమేజింగ్ అప్లికేషన్లకు బాగా సరిపోతాయి.
“ఈ పని లేబుల్-ఫ్రీ మెటబాలిక్ ఇమేజింగ్ కోసం డెప్త్ పెనెట్రేషన్ పరంగా గణనీయమైన మెరుగుదలను చూపుతుంది. ఇది జీవన జీవవ్యవస్థలలో లోతుగా జీవక్రియ డైనమిక్లను అధ్యయనం చేయడానికి మరియు అన్వేషించడానికి కొత్త మార్గాలను తెరుస్తుంది” అని ఎలక్ట్రికల్ ఇంజనీరింగ్ మరియు కంప్యూటర్ సైన్స్ విభాగంలో అసిస్టెంట్ ప్రొఫెసర్ సిక్సియన్ యు చెప్పారు. (EECS), రీసెర్చ్ లాబొరేటరీ ఫర్ ఎలక్ట్రానిక్స్ సభ్యుడు మరియు ఈ ఇమేజింగ్ పై ఒక పేపర్ యొక్క సీనియర్ రచయిత సాంకేతికత.
ఆమె EECS గ్రాడ్యుయేట్ విద్యార్థి అయిన ప్రధాన రచయిత కుంజాన్ లియు ద్వారా కాగితంపై చేరారు; టోంగ్ క్యూ, ఒక MIT పోస్ట్డాక్; Honghao Cao, EECS గ్రాడ్యుయేట్ విద్యార్థి; ఫ్యాన్ వాంగ్, బ్రెయిన్ అండ్ కాగ్నిటివ్ సైన్సెస్ ప్రొఫెసర్; రోజర్ కమ్, సెసిల్ మరియు ఇడా గ్రీన్ బయోలాజికల్ అండ్ మెకానికల్ ఇంజినీరింగ్ విశిష్ట ప్రొఫెసర్; లిండా గ్రిఫిత్, స్కూల్ ఆఫ్ ఇంజనీరింగ్ ప్రొఫెసర్ ఆఫ్ టీచింగ్ ఇన్నోవేషన్ డిపార్ట్మెంట్ ఆఫ్ బయోలాజికల్ ఇంజనీరింగ్; మరియు ఇతర MIT సహచరులు. పరిశోధన ఈ రోజు కనిపిస్తుంది సైన్స్ అడ్వాన్స్లు .
లేజర్-కేంద్రీకృత
ఈ కొత్త పద్ధతి లేబుల్-ఫ్రీ ఇమేజింగ్ వర్గంలోకి వస్తుంది, అంటే కణజాలం ముందుగా తడిసినది కాదు. స్టెయినింగ్ వ్యత్యాసాన్ని సృష్టిస్తుంది, ఇది కణ కేంద్రకాలు మరియు ప్రోటీన్లను మెరుగ్గా చూడడానికి క్లినికల్ బయాలజిస్ట్కి సహాయపడుతుంది. కానీ మరకకు సాధారణంగా జీవశాస్త్రవేత్త నమూనాను విభజించి ముక్కలు చేయవలసి ఉంటుంది, ఈ ప్రక్రియ తరచుగా కణజాలాన్ని చంపుతుంది మరియు జీవ కణాలలో డైనమిక్ ప్రక్రియలను అధ్యయనం చేయడం అసాధ్యం చేస్తుంది.
లేబుల్-రహిత ఇమేజింగ్ పద్ధతులలో, పరిశోధకులు కణాలలోని నిర్దిష్ట అణువులను ప్రకాశవంతం చేయడానికి లేజర్లను ఉపయోగిస్తారు, తద్వారా అవి వివిధ పరమాణు విషయాలు మరియు సెల్యులార్ నిర్మాణాలను బహిర్గతం చేసే వివిధ రంగుల కాంతిని విడుదల చేస్తాయి. అయినప్పటికీ, డీప్-టిష్యూ ఇమేజింగ్ కోసం నిర్దిష్ట తరంగదైర్ఘ్యాలు మరియు అధిక-నాణ్యత పప్పులతో ఆదర్శ లేజర్ కాంతిని ఉత్పత్తి చేయడం సవాలుగా ఉంది.
ఈ పరిమితిని అధిగమించడానికి పరిశోధకులు కొత్త విధానాన్ని అభివృద్ధి చేశారు. వారు ఒక మల్టీమోడ్ ఫైబర్ను ఉపయోగిస్తారు, ఇది ఒక రకమైన ఆప్టికల్ ఫైబర్, ఇది గణనీయమైన శక్తిని కలిగి ఉంటుంది మరియు దానిని “ఫైబర్ షేపర్” అని పిలిచే ఒక కాంపాక్ట్ పరికరంతో జత చేస్తుంది. ఫైబర్ యొక్క ఆకారాన్ని అనుకూలంగా మార్చడం ద్వారా కాంతి ప్రచారాన్ని ఖచ్చితంగా మాడ్యులేట్ చేయడానికి ఈ షేపర్ వారిని అనుమతిస్తుంది. ఫైబర్ను వంచడం వల్ల లేజర్ యొక్క రంగు మరియు తీవ్రత మారుతుంది.
మునుపటి పని ఆధారంగా, పరిశోధకులు లోతైన మల్టీమోడల్ మెటబాలిక్ ఇమేజింగ్ కోసం ఫైబర్ షేపర్ యొక్క మొదటి సంస్కరణను స్వీకరించారు.
“మేము ఈ శక్తిని మనకు అవసరమైన పల్స్ లక్షణాలతో మనకు అవసరమైన రంగులలోకి మార్చాలనుకుంటున్నాము. ఇది కణజాలాలలో లోతుగా కూడా అధిక తరం సామర్థ్యాన్ని మరియు స్పష్టమైన చిత్రాన్ని ఇస్తుంది” అని కావో చెప్పారు.
వారు నియంత్రించదగిన యంత్రాంగాన్ని నిర్మించిన తర్వాత, కాంతి యొక్క పొడవైన తరంగదైర్ఘ్యాలను ఉత్పత్తి చేయడానికి శక్తివంతమైన లేజర్ మూలాన్ని ప్రభావితం చేయడానికి వారు ఇమేజింగ్ ప్లాట్ఫారమ్ను అభివృద్ధి చేశారు, ఇవి జీవ కణజాలాలలోకి లోతుగా చొచ్చుకుపోవడానికి కీలకమైనవి.
“ఈ సాంకేతికత జీవశాస్త్ర పరిశోధనలను గణనీయంగా ముందుకు తీసుకెళ్లగల సామర్థ్యాన్ని కలిగి ఉందని మేము విశ్వసిస్తున్నాము. జీవశాస్త్ర ప్రయోగశాలలకు సరసమైన మరియు అందుబాటులో ఉండేలా చేయడం ద్వారా, ఆవిష్కరణ కోసం శక్తివంతమైన సాధనంతో శాస్త్రవేత్తలను శక్తివంతం చేయాలని మేము ఆశిస్తున్నాము” అని లియు చెప్పారు.
డైనమిక్ అప్లికేషన్లు
పరిశోధకులు వారి ఇమేజింగ్ పరికరాన్ని పరీక్షించినప్పుడు, కాంతి 700 మైక్రోమీటర్ల కంటే ఎక్కువ జీవ నమూనాలోకి చొచ్చుకుపోగలిగింది, అయితే ఉత్తమ మునుపటి పద్ధతులు 200 మైక్రోమీటర్లకు మాత్రమే చేరుకోగలవు.
“ఈ కొత్త రకం డీప్ ఇమేజింగ్తో, మేము జీవ నమూనాలను చూడాలనుకుంటున్నాము మరియు మనం ఇంతకు ముందెన్నడూ చూడని వాటిని చూడాలనుకుంటున్నాము” అని లియు జతచేస్తుంది.
లోతైన ఇమేజింగ్ టెక్నిక్ వాటిని జీవన వ్యవస్థలో బహుళ స్థాయిలలో కణాలను చూడడానికి వీలు కల్పించింది, ఇది వివిధ లోతుల వద్ద జరిగే జీవక్రియ మార్పులను అధ్యయనం చేయడంలో పరిశోధకులకు సహాయపడుతుంది. అదనంగా, వేగవంతమైన ఇమేజింగ్ వేగం సెల్ యొక్క జీవక్రియ దాని కదలికల వేగం మరియు దిశను ఎలా ప్రభావితం చేస్తుందనే దానిపై మరింత వివరణాత్మక సమాచారాన్ని సేకరించడానికి అనుమతిస్తుంది.
ఈ కొత్త ఇమేజింగ్ పద్ధతి ఆర్గానాయిడ్ల అధ్యయనానికి ప్రోత్సాహాన్ని అందిస్తుంది, ఇవి అవయవాల నిర్మాణం మరియు పనితీరును అనుకరించేలా పెరిగే ఇంజనీరింగ్ కణాలు. కమ్ మరియు గ్రిఫిత్ ల్యాబ్లలోని పరిశోధకులు మెదడు మరియు ఎండోమెట్రియల్ ఆర్గానాయిడ్ల అభివృద్ధికి మార్గదర్శకత్వం వహించారు, ఇవి వ్యాధి మరియు చికిత్స అంచనా కోసం అవయవాల వలె పెరుగుతాయి.
అయినప్పటికీ, కణజాలాన్ని కత్తిరించకుండా లేదా మరక చేయకుండా అంతర్గత పరిణామాలను ఖచ్చితంగా గమనించడం సవాలుగా ఉంది, ఇది నమూనాను చంపుతుంది.
ఈ కొత్త ఇమేజింగ్ టెక్నిక్, అది పెరుగుతూనే ఉండగా, జీవక్రియలోని జీవక్రియ స్థితులను నాన్వాసివ్గా పర్యవేక్షించడానికి పరిశోధకులను అనుమతిస్తుంది.
వీటిని మరియు ఇతర బయోమెడికల్ అప్లికేషన్లను దృష్టిలో ఉంచుకుని, పరిశోధకులు మరింత ఎక్కువ రిజల్యూషన్ ఉన్న చిత్రాల కోసం లక్ష్యంగా పెట్టుకున్నారు. అదే సమయంలో, వారు తక్కువ-నాయిస్ లేజర్ మూలాలను రూపొందించడానికి పని చేస్తున్నారు, ఇది తక్కువ కాంతి మోతాదుతో లోతైన ఇమేజింగ్ను ప్రారంభించగలదు.
వారు అధిక రిజల్యూషన్లో జీవ నమూనాల పూర్తి 3D నిర్మాణాలను పునర్నిర్మించడానికి చిత్రాలకు ప్రతిస్పందించే అల్గారిథమ్లను కూడా అభివృద్ధి చేస్తున్నారు.
దీర్ఘకాలంలో, కొత్త ఔషధాల అభివృద్ధిలో సహాయపడటానికి జీవశాస్త్రజ్ఞులు ఔషధ ప్రతిస్పందనను నిజ సమయంలో పర్యవేక్షించడంలో సహాయపడటానికి వాస్తవ ప్రపంచంలో ఈ సాంకేతికతను వర్తింపజేయాలని వారు ఆశిస్తున్నారు.
“కణజాలంలోకి లోతుగా చేరే మల్టీమోడల్ మెటబాలిక్ ఇమేజింగ్ను ప్రారంభించడం ద్వారా, మేము శాస్త్రవేత్తలకు వారి సహజ స్థితిలో పారదర్శకంగా లేని జీవ వ్యవస్థలను గమనించే అపూర్వమైన సామర్థ్యాన్ని అందిస్తున్నాము. దీని సరిహద్దులను ముందుకు తీసుకురావడానికి వైద్యులు, జీవశాస్త్రవేత్తలు మరియు బయో ఇంజనీర్లతో సహకరించడానికి మేము సంతోషిస్తున్నాము. సాంకేతికత మరియు ఈ అంతర్దృష్టులను వాస్తవ ప్రపంచ వైద్య పురోగతులుగా మార్చండి” అని మీరు చెప్పారు.
“ఈ పని ఉత్తేజకరమైనది ఎందుకంటే ఇది ప్రస్తుత పద్ధతులతో పోలిస్తే కణజాలంలో కణ జీవక్రియను లోతుగా చిత్రించడానికి వినూత్న అభిప్రాయ పద్ధతులను ఉపయోగిస్తుంది. ఈ సాంకేతికతలు వేగవంతమైన ఇమేజింగ్ వేగాన్ని కూడా అందిస్తాయి, ఇది రక్త నాళాలలో రోగనిరోధక కణ చలనశీలత యొక్క ప్రత్యేకమైన జీవక్రియ డైనమిక్లను వెలికితీసేందుకు ఉపయోగించబడింది. ఈ ఇమేజింగ్ టూల్స్ డైనమిక్ లివింగ్ సిస్టమ్స్లో సెల్ ఫంక్షన్ మరియు మెటబాలిజం మధ్య లింక్లను కనుగొనడంలో ఉపకరిస్తాయి” అని చెప్పారు. మెలిస్సా స్కాలా, మోర్గ్రిడ్జ్ ఇన్స్టిట్యూట్ ఫర్ రీసెర్చ్లోని పరిశోధకురాలు, ఈ పనిలో పాల్గొనలేదు.
“NAD(P)H ఆటోఫ్లోరోసెన్స్ కాంట్రాస్ట్పై ఆధారపడిన అధిక రిజల్యూషన్ మల్టీ-ఫోటాన్ ఇమేజ్లను వేగంగా మరియు లోతుగా కణజాలంలోకి పొందడం ద్వారా అనేక రకాల ముఖ్యమైన సమస్యల అధ్యయనానికి తలుపులు తెరుస్తుంది” అని బయోమెడికల్ ఇంజనీరింగ్ ప్రొఫెసర్ ఐరీన్ జార్గకౌడి జతచేస్తుంది టఫ్ట్స్ విశ్వవిద్యాలయం కూడా ఈ పనిలో పాల్గొనలేదు. “మీరు జీవక్రియ పనితీరును అంచనా వేసినప్పుడల్లా జీవ కణజాలాలను వీలైనంత వేగంగా చిత్రించడం అనేది డేటా యొక్క శారీరక ఔచిత్యాన్ని నిర్ధారించడం, అర్థవంతమైన కణజాల వాల్యూమ్ను శాంపిల్ చేయడం లేదా వేగవంతమైన మార్పులను పర్యవేక్షించడం వంటి అంశాలలో ఎల్లప్పుడూ భారీ ప్రయోజనం. క్యాన్సర్ నిర్ధారణ లేదా న్యూరోసైన్స్, ఇమేజింగ్లో లోతైన – మరియు వేగంగా – ఇంతకు ముందు సజీవ కణజాలాలలో అధ్యయనం చేయని ధనిక సమస్యలు మరియు పరస్పర చర్యలను పరిగణనలోకి తీసుకునేలా చేస్తుంది.”